Maglev Artificial Heart Pump and Experimental Study on ECMO
-
摘要:
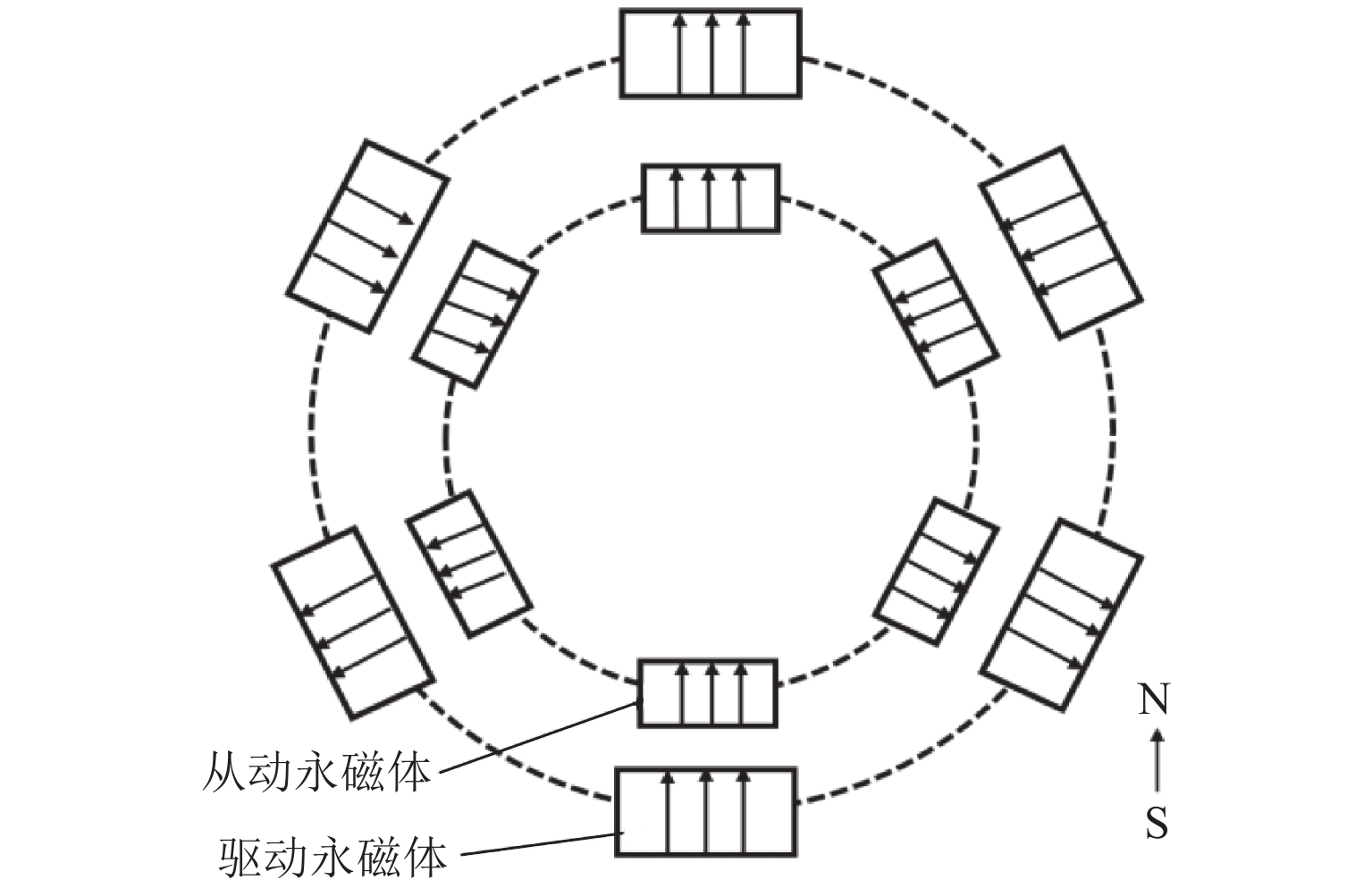
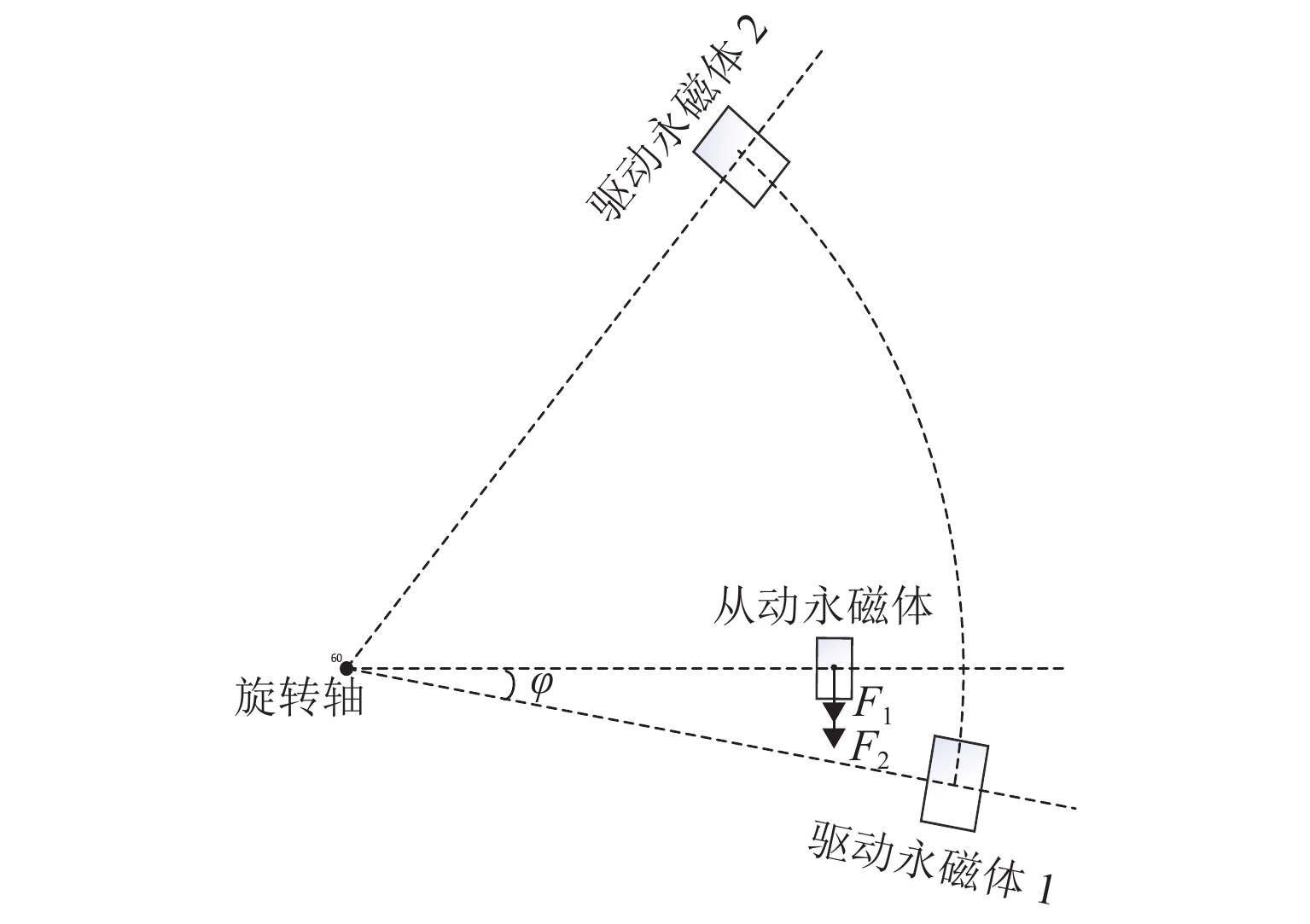
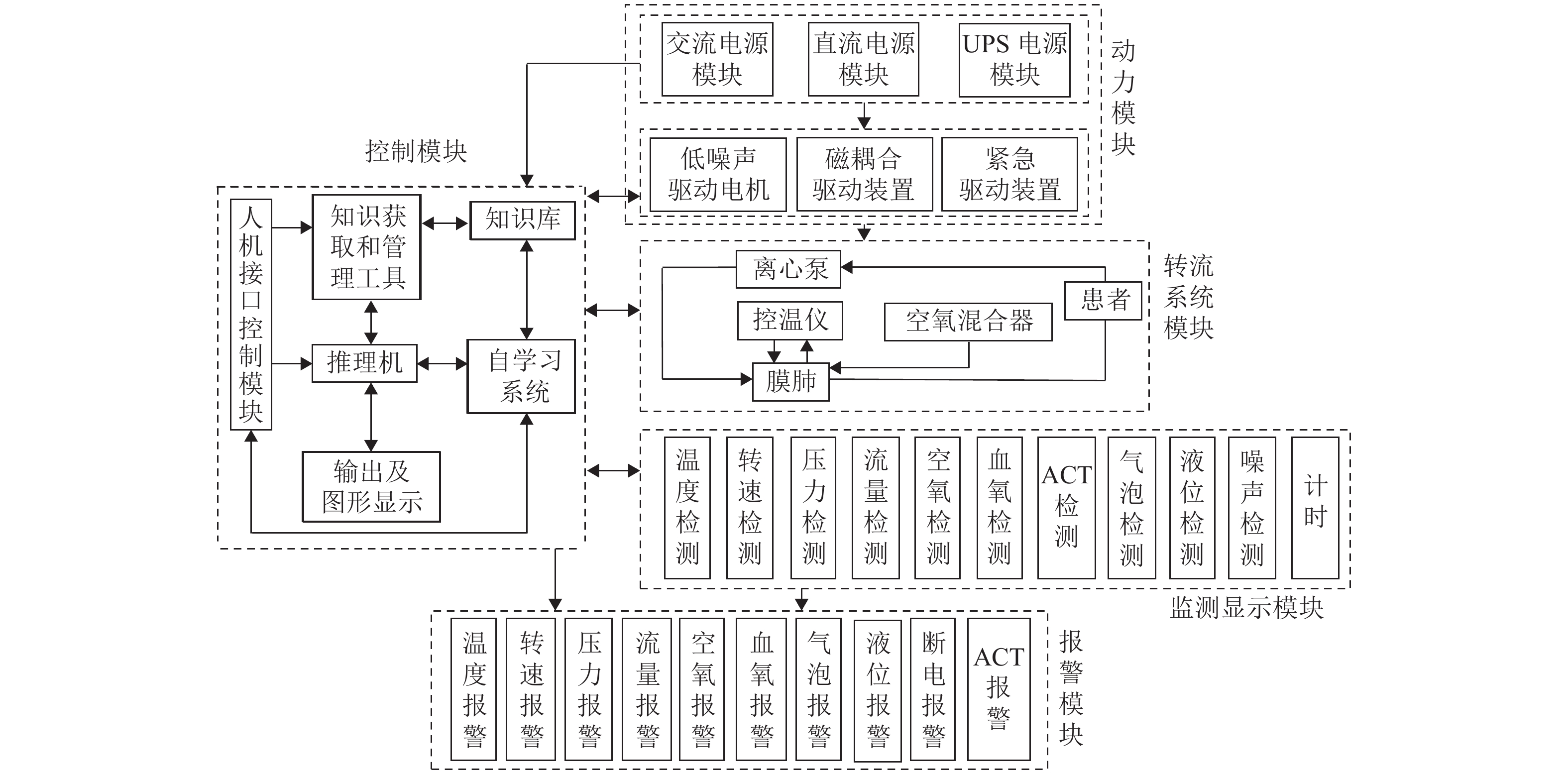
体外循环生命支持系统(extracorporeal membrane oxygenation,ECMO)可替代人的心、肺工作,为挽救生命创造机会,在这次抗击新冠疫情中屡建奇功,被称为“救命神器”. 针对作为ECMO动力源的磁悬浮人工心脏泵,本文对其磁悬浮系统和无接触高效率磁耦合驱动装置进行了研究;在多入多出智能控制系统控制下实现了磁悬浮人工心脏泵变速稳定运行,并开展了磁悬浮人工心脏泵的压力、流量和转速实验;用所研制的磁悬浮人工心脏泵进行了3 d的动物实验后自主撤机. 研究结果表明:体外循环磁悬浮离心血泵表现出良好的稳定运行特性,保持转速不变,在流量变化较大时,进出口压力差变化不大;体外循环磁悬浮离心血泵在转速为5000 r/min时,进出口压力差可以达到750 mmHg,具有较宽的工况范围;持续进行了15 d可靠性试验后,各项测试参数符合特性曲线规律;试验期间,羊生命体征持续存在,撤机后羊的生命体征平稳,验证了所研发的磁悬浮人工心脏泵在ECMO系统上应用的有效性和安全性.
Abstract:Extracorporeal membrane oxygenation (ECMO) can replace human heart and lung work and create opportunities to save lives. ECMO has made outstanding achievements in defending against the novel coronavirus pneumonia and has thus been called a lifesaving appliance. In view of the power source of ECMO, namely the maglev artificial heart pump, its maglev system and contactless high-efficiency magnetic coupling driver were studied. The maglev artificial heart pump was controlled by a multi-input and multi-output intelligent control system to realize variable speed and stable operation. The experiments of pressure, flow, and speed of the maglev artificial heart pump were carried out. The developed maglev artificial heart pump was used for three days of animal experiments and active withdrawal. The results show that the extracorporeal maglev centrifugal pump shows excellent stable operation characteristics and keeps the speed unchanged; the pressure difference between the inlet and outlet does not change much when the flow rate varies greatly. The pressure difference between the inlet and outlet of the extracorporeal maglev centrifugal pump can reach 750 mmHg at a speed of 5 000 r/min, which has a wide working range. After 15 days of continuous reliability experiments, all test parameters conform to the law of characteristic curves. During the test, the vital signs of the sheep were monitored and were stable after the machine was removed, which verified the effectiveness and safety of the developed maglev artificial heart pump applied in ECMO.
-
Key words:
- maglev /
- artificial heart pump /
- magnetic coupling /
- ECMO
-
表 1 钕铁硼N52参数
Table 1. Parameters of neodymium iron boron N52
规格 剩磁/T 矫顽力/
( kA·m−1)内禀矫顽力/
( kA·m−1)最大剩磁积/
(kJ·m−3)工作温度/℃ N52 1.42~
1.49≥835 ≥876 390~422 ≤80 -
[1] 于坤,黑飞龙. 我国体外循环发展面临的挑战与机遇[J]. 中华医学杂志,2017,97(38): 2961-2962. doi: 10.3760/cma.j.issn.0376-2491.2017.38.001YU Kun, HEI Feilong. Challenges and opportunities faced by the development of cardiopulmonary bypass in China[J]. National Medical Journal of China, 2017, 97(38): 2961-2962. doi: 10.3760/cma.j.issn.0376-2491.2017.38.001 [2] PETROU A, KUSTER D, LEE J, et al. Comparison of flow estimators for rotary blood pumps: an in vitro and in vivo study[J]. Annals of Biomedical Engineering, 2018, 46(12): 2123-2134. doi: 10.1007/s10439-018-2106-7 [3] 陈凯,唐汉韡,侯剑峰,等. 体外膜肺氧合在心脏外科领域的应用[J]. 中国循环杂志,2019,34(12): 1244-1248. doi: 10.3969/j.issn.1000-3614.2019.12.020CHEN Kai, TANG Han, HOU Jianfeng, et al. Application of extracorporeal membrane oxygenation in cardiac surgery[J]. Chinese Circulation Journal, 2019, 34(12): 1244-1248. doi: 10.3969/j.issn.1000-3614.2019.12.020 [4] 盖玉彪,赵丽,于雅洁,等. 应用ECMO技术救治重症肺炎患者的护理体会[J]. 当代护士(专科版),2019,26(11): 89-91. [5] 赵文君, 胡浩, 李思远. “ECMO”紧急大驰援——一切为了重症患者的救治[N]. 新华社, 2020-3-18. [6] 潘佳秀子, 李晗. 武大中南医院: 用ECMO技术成功救治一新型冠状病毒肺炎患者[N]. 中国青年网, 2020-01-22. [7] 田荣成,刘抗,张泽生,等. 体外膜肺氧合技术(ECMO)在临床急危重症医学的应用进展[J]. 赣南医学院学报,2019,39(12): 1207-1212.TIAN Rongcheng, LIU Kang, ZHANG Zesheng, et al. Advances in the application of extracorporeal membrane oxygenation (ECMO) in clinical critical and critical medicine[J]. Journal of Gannan Medical University, 2019, 39(12): 1207-1212. [8] 崔永超, 杜中涛, 江春景, 等. 体外心肺复苏在成人难治性院内心脏骤停中的应用[J/OL]. 中华损伤与修复杂志(电子版), 2019, 14(2): 108-112. https://zhssyxfzz.cma-cmc.com.cn/CN/article/advancedSearchResult.do.CUI Yongchao, DU Zhongtao, JIANG Chunjing, et al. Application of extracorporeal cardiopulmonary resuscitation in refractory in-hospital cardiac arrest in adults[J/OL]. Chinese Journal of Injury Repair and Wound Healing (Electronic Edition), 2019, 14(2): 108-112. https://zhssyxfzz.cma-cmc.com.cn/CN/article/advancedSearchResult.do. [9] 山东大学. 应用于离心式人工心脏泵的单端轴向分离式磁悬浮轴承: ZL 201510284041.2[P]. 2017-03-22. [10] 东莞科威医疗器械有限公司. 一种膜式氧合器: CN107485744B[P]. 2019-08-30. [11] 四川大学. 用于体外膜肺氧合(ECMO)的长效膜式氧合器中空纤维抗凝涂层及制备方法: 中国, CN111760077B[P]. 2021-03-30. [12] 赵思鹏. 体外离心式磁悬浮血泵的控制与试验研究[D]. 济南: 山东大学, 2020. [13] 山东大学. 一种VV-ECMO模式下血氧饱和度控制系统及设备: 202010968392.6[P]. 2021-06-28. [14] 刘淑琴. 磁悬浮位移测量技术[M]. 北京: 科学出版社, 2019: 93-94. [15] THAMSEN B, BLÜMEL B, SCHALLER J, et al. Numerical analysis of blood damage potential of the HeartMate Ⅱ and HeartWare HVAD rotary blood pumps[J]. Artificial Organs, 2015, 39(8): 651-659. doi: 10.1111/aor.12542 [16] UKITA R, WU K, LIN X J, et al. Zwitterionic poly-carboxybetaine coating reduces artificial lung thrombosis in sheep and rabbits[J]. Acta Biomaterialia, 2019, 92: 71-81. doi: 10.1016/j.actbio.2019.05.019 [17] LIU S Q, BIAN Z G, FAN Y P, et al. Zero-power control for magnetic bearings in artificial heart pumps[C]//ISMB14. Linz: [s.n.], 2014: 11-14. [18] 胡磊青,程军,王亚丽,等. PVP改性PDMS/PAN中空纤维复合膜提升表面亲水性[J]. 浙江大学学报(工学版),2019,53(2): 228-233. doi: 10.3785/j.issn.1008-973X.2019.02.004HU Leiqing, CHENG Jun, WANG Yali, et al. Improvement on surface hydrophily of hollow fiber-supported PDMS gas separation membrane by PVP modification[J]. Journal of Zhejiang University (Engineering Science), 2019, 53(2): 228-233. doi: 10.3785/j.issn.1008-973X.2019.02.004 [19] 国家药品监督管理局. 医疗器械临床前动物研究第1部分, 通用要求: YY/T 1754.1—2020[S]. 北京: 中国标准出版社, 2020. [20] 侯晓彤. 规范发展体外膜氧合循环辅助支持[J]. 中国体外循环杂志,2018,16(4): 193-195. doi: 10.13498/j.cnki.chin.j.ecc.2018.04.01HOU Xiaotong. Standardize the development of extracorporeal membrane oxygenation circulation auxiliary support[J]. Chinese Journal of Extracorporeal Circulation, 2018, 16(4): 193-195. doi: 10.13498/j.cnki.chin.j.ecc.2018.04.01 [21] 章晓华,庄建. 中国体外膜肺氧合技术开展的现状及思考[J]. 中国体外循环杂志,2017,15(2): 68-71,91. doi: 10.13498/j.cnki.chin.j.ecc.2017.02.02ZHANG Xiaohua, ZHUANG Jian. Present situation and thinking of extracorporeal membrane oxygenation technology in China[J]. Chinese Journal of Extracorporeal Circulation, 2017, 15(2): 68-71,91. doi: 10.13498/j.cnki.chin.j.ecc.2017.02.02 [22] 刘伟,卢帝君. 体外循环心肺复苏在急诊心脏骤停患者抢救中的临床应用[J]. 中国临床医生杂志,2019,47(1): 8-10. doi: 10.3969/j.issn.2095-8552.2019.01.003LIU Wei, LU Dijun. Clinical application of cardiopulmonary resuscitation with cardiopulmonary bypass in emergency cardiac arrest patients[J]. Chinese Journal for Clinicians, 2019, 47(1): 8-10. doi: 10.3969/j.issn.2095-8552.2019.01.003 -




 下载:
下载: